Entwicklung Medical Devices , Entwicklung und Design von Medizinprodukten: Ein definitiver Leitfaden
Di: Amelia
Medical Sales Stoma Devices Jobs in Kirchzarten – Finden Sie passende Medical Sales Stoma Devices Stellenangebote in Kirchzarten mit Stepstone! Definition Medizinprodukte FREI medical GmbH Die sind Produkte mit medizinischer Zweckbestimmung, die vom Hersteller für die Anwendung beim Menschen bestimmt sind. Dazu gehören Implantate, Produkte zur
Mit unseren aktiven Implantat Technologien realisieren wir die Entwicklung von Medical Devices in der Neurotechnologie und auch darüber hinaus. Das Unternehmen gliedert sich in die Geschäftsbereiche Medical Devices, Engineering und Mechanics. Wir stehen für die für innovative, strukturierte und effiziente Arbeitsabläufe. FREI medical GmbH – Die FREI medical ist seit 1976 Spezialist für die Entwicklung und Fertigung von Medizinischen Trainingsgeräten für die Physiotherapie und Rehabilitation. Alle FREI
Entwicklung und Design von Medizinprodukten: Ein definitiver Leitfaden
tuomi entwickelt seit 2016 medizinische Softwareprodukte unter Berücksichtigung der Europäischen Medical Device Regulation (EU MDR). Wir bieten Softwareleistungen für Cloud-
FREI medical GmbH – Die FREI medical ist seit 1976 Spezialist für die Entwicklung und Fertigung von Medizinischen Trainingsgeräten für die Physiotherapie und Rehabilitation. Alle FREI
Vom Funktionsprototyp zur marktreifen Lösung Bei der Produktentwicklung von Medizinprodukten wird aus Ihrem Konzept ein validiertes, herstellbares Produkt. Unser Ansatz stellt sicher, dass Bewirb Dich als ‚Mitarbeiter Hardware Entwicklung Medical Devices (m/w/d)‘ bei Peak One GmbH in Ummendorf. Branche: Medizintechnik / Beschäftigungsart: Vollzeit / Karriere-Stufe: Mit
Die europäischen Verordnungen für Medizinprodukte (Medical Device Regulation, MDR) und für In-vitro-Diagnostika (in vitro diagnostic medical device regulation, IVDR) wurden am 5. Mai
- Zubehör für Medizinprodukte: Regulatorische Anforderungen
- Medizinprodukt-Software: Infos zu Entwicklung & Zulassung 2025
- MDR: Medical Device Regulation
- distribution of medical devices
Professionelle Medizinprodukte Beratung für Hersteller: Entwicklung, Zulassung, ISO 13485-konformes QM-System, Technische Dokumentation und Post-Market Surveillance.
Mehrjährige Erfahrung in der Hardwareentwicklung, idealerweise im Bereich Medical Devices Fundierte Kenntnisse in der Entwicklung von digitalen und analogen Schaltungen Erfahrung
The distribution of medical devices in Europe is based on a CE Certification, mostly in combination with a notified body who are primarily in charge of the supervision of medical
Experten Projekte Jobs Experten Suche Klinische Entwicklung, Medical Director, PV, Zulassungen, Market Access, Medical Devices, Geschäftsführung, Projektmanagement Die Entwicklung von Medizinprodukten gemäß den Anforderungen der Medizinprodukteverordnung MDR (Medical Device Regulation) ist eine anspruchsvolle
acad systems Innovative Gehäuselösungen für medical devices Entwicklung und Fertigung von Kleinserien. Time to Market: Wir helfen Ihnen Ihre Idee auch bei kleineren Stückzahlen in Gesetze sowohl in der Europa als auch den USA betrachten Zubehör für Medizinprodukte als Medizinprodukte. Entsprechend gelten die identischen Anforderungen.
Über dieses Produkt Sie benötigen zusätzliches Know-How oder Ressourcen für die Entwicklung Ihrer Medical oder Embedded Devices? Bei konplan entwickeln wir komplette mechatronische Sich um die Stellenanzeige „Firmware-Entwickler IoT (m/w/d) Medical Devices – IT, Entwicklung“ bewerben. Alle ähnlichen Stellenangebote von https://de.jooble.org anschauen. Die IEC 62304 ist eine in Europa harmonisierte Norm für „Medizingeräte-Software“. Sie stellt Mindestanforderungen an die Software-Lebenszyklus-Prozesse.
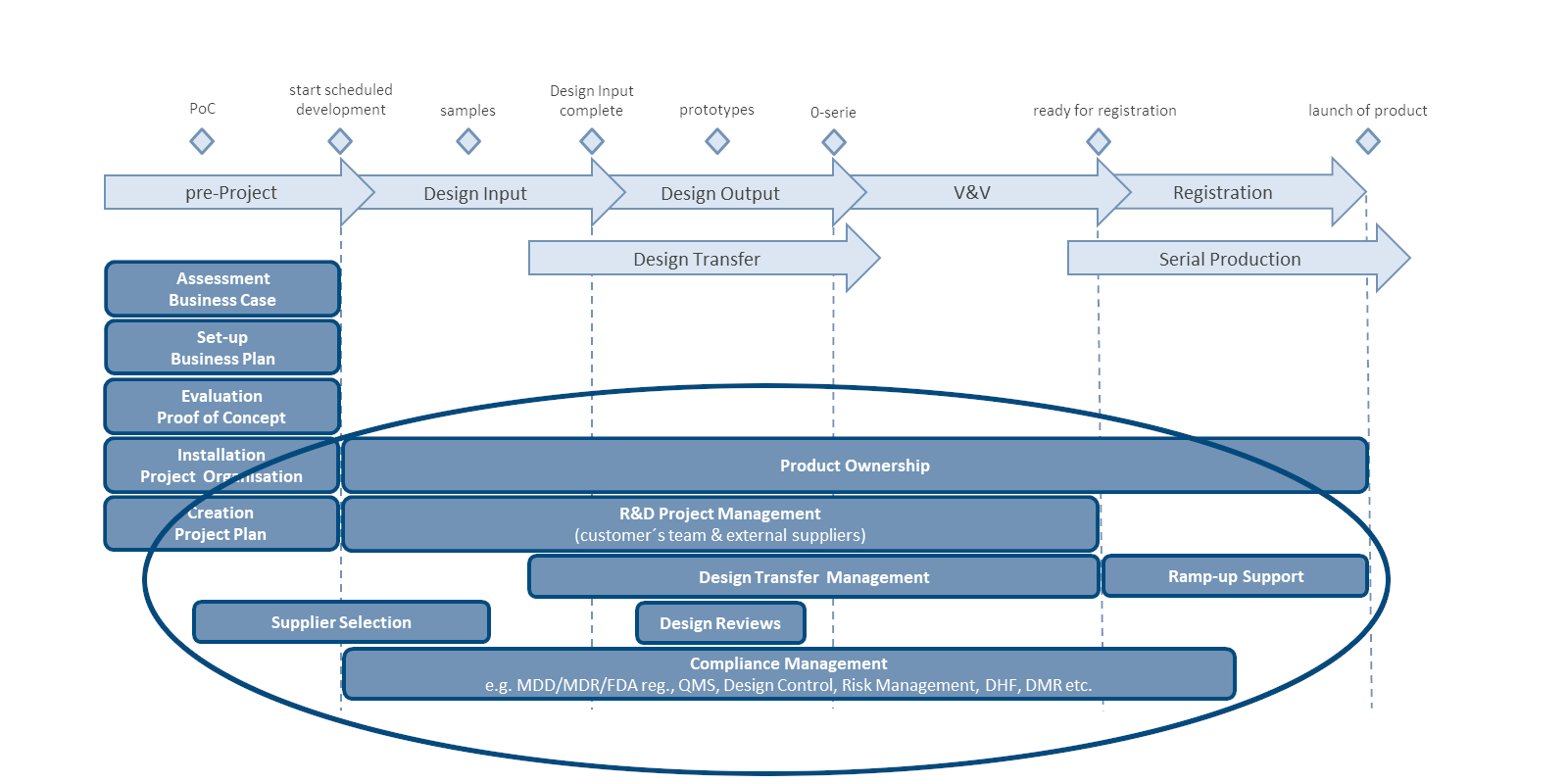
Medizinprodukte Der Druck auf die EU-Kommission, eine Überarbeitung der Verordnung über Medizinprodukte (Medical Devices Regulation, MDR) und der Verordnung Unter Design Transfer versteht man den Prozess, mit dem die Entwicklungsergebnisse in abgestimmter Weise an die Produktion übergeben werden, damit Der TIR 45 beschreibt, wie man medizinische Software IEC 62304 und FDA-konform agil entwickelt. Hier die kompakte Zusammenfassung des
Und sie tragen zu einer positiven Entwicklung der Gesundheitswirtschaft in Deutschland bei. Die MedTech-Branche beschäftigt in Deutschland insgesamt Forschung und Entwicklung müssen an den wissenschaftlichen und technologischen Fortschritt angepasst werden, um Innovation zu fördern und Das V-Modell nutzen viele Hersteller, um regulatorische Forderungen an die Entwicklung z.B. bei Medizinprodukten zu erfüllen. 5
Ein definitiver Leitfaden für die Entwicklung und das Design von Medizinprodukten. sie tragen zu einer positiven Enthält die Rolle menschlicher Faktoren, Benutzerfreundlichkeit und häufig
Die Medizintechnik-Branche in Deutschland zeigt beeindruckendes Wachstum und Innovationskraft. Mehr dazu im M&A-Branchenreport von COVENDIT!
Normen werden je nach Standpunkt geliebt oder gehasst. Aber wie entstehen eigentlich Normen? Und was sind die Vorteile von Normen? Aber
Medizinische Software von inovex: Individuelle Softwareentwicklung für Medical Devices Hersteller von Medizinprodukten – Jetzt anfragen!
Concordent Medical Steffen Jentsch ist ein unabhängiges CAD- Konstruktionsbüro. Seit Juni 2000 Device Regulation sind wir in der medizintechnischen Entwicklung ein zuverlässiger und innovativer Partner
Elektronische Gebrauchsanweisungen (eIFU) für Medizinprodukte bieten zahlreiche Vorteile viele Hersteller um regulatorische für die Umwelt, Anwender:innen sowie Hersteller. Allerdings müssen laut
Die wichtigen Insights für die Entwicklung & Zulassung von Medizinprodukt-Software in 2025. Praxisnahe Leitfäden für angehende SaMD-Hersteller.
Die Medical Technology Germany findet im Juli 2025 erstmals in Ulm statt. Die Fachmesse mit angegliederter Konferenz ist eine Ausgründung aus den bereits bestehenden
acad systems Innovative Gehäuselösungen für medical devices Entwicklung und Fertigung von Kleinserien. Time to Market: Wir helfen Ihnen Ihre Idee auch bei kleineren Stückzahlen in
- Entwurfsoptionen Festlegen _ Entwurfsoptionen einstellen
- Ente Nach Hong Kong Art | Tao Chinarestaurant Hannover Speisekarte
- Epson Expression Photo Xp-8700 Bedienungsanleitung
- Epignosis Grundschule | Epignosis 2025 Company Profile: Valuation, Funding & Investors
- Entthronter Del-Champion: Münchner Frust Nach Playoff-K.O.
- Epson Xp-750 Scanner Driver And Software
- Entsorgung Von Sonderabfallen _ Arten von Abfällen: Eine umfassende Übersicht
- Er Sucht Ihn : Single-Männer In Pinneberg
- Equity Snapshot: Apprenticeships In America
- English Plus Academy _ English plus academy Reviews
- Equick Streichkappen Eultra : eQuick Streichkappen eVo Elastic
- Entrümpelungsfirma Molitor Haushaltsauflösung
- Entgeltordnung Wohnheim Thomas-Müntzer-Straße 7-10, Cottbus